[Uso previsto]
La prueba rápida de troponina I (cTnI) (sangre entera/suero/plasma) es una prueba de inmunología visual rápida para la detección presuntiva cualitativa de troponina I cardíaca en sangre entera humana.muestras de suero o plasmaEstá destinado para su uso como ayuda en el diagnóstico del infarto de miocardio (IM).
[Introducción]
La troponina cardíaca I (cTnI) es una proteína que se encuentra en el músculo cardíaco con un peso molecular de 22,5 kDa.Junto con la tropomiosina, este complejo estructural forma el componente principal que regula la actividad de la ATPasa sensible al calcio de la actomiosina en el músculo esquelético estriado y el músculo cardíaco.La troponina I se libera en la sangre de 4 a 6 horas después del inicio del dolorEl patrón de liberación de cTnI es similar al de CK-MB, pero mientras que los niveles de CK-MB vuelven a la normalidad después de 72 horas, la troponina I permanece elevada durante 6 a 10 días.lo que permite una ventana de detección más larga para la lesión cardíacaLa alta especificidad de las mediciones de cTnI para la identificación de daños miocárdicos se ha demostrado en condiciones tales como el período perioperatorio, después de carreras de maratón,y traumatismo en el pecho. la liberación de cTnI también se ha documentado en enfermedades cardíacas distintas del infarto agudo del miocardio (AMI), como angina inestable, insuficiencia cardíaca congestiva,y daño isquémico debido a la cirugía de bypass de la arteria coronariaDebido a su alta especificidad y sensibilidad en el tejido miocárdico, la troponina I se ha convertido recientemente en el biomarcador preferido para el infarto de miocardio.
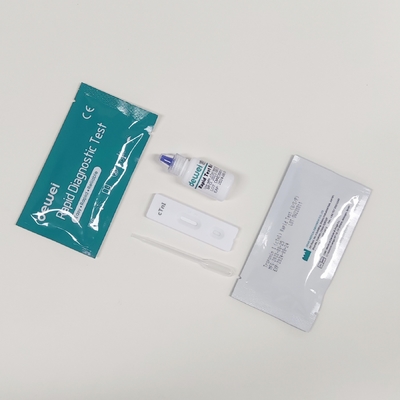
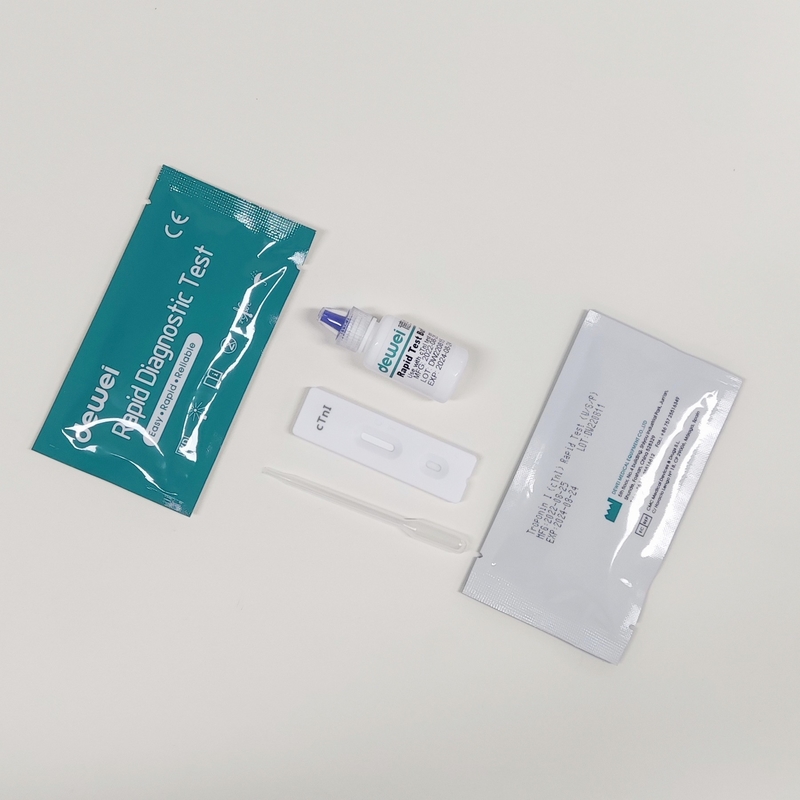
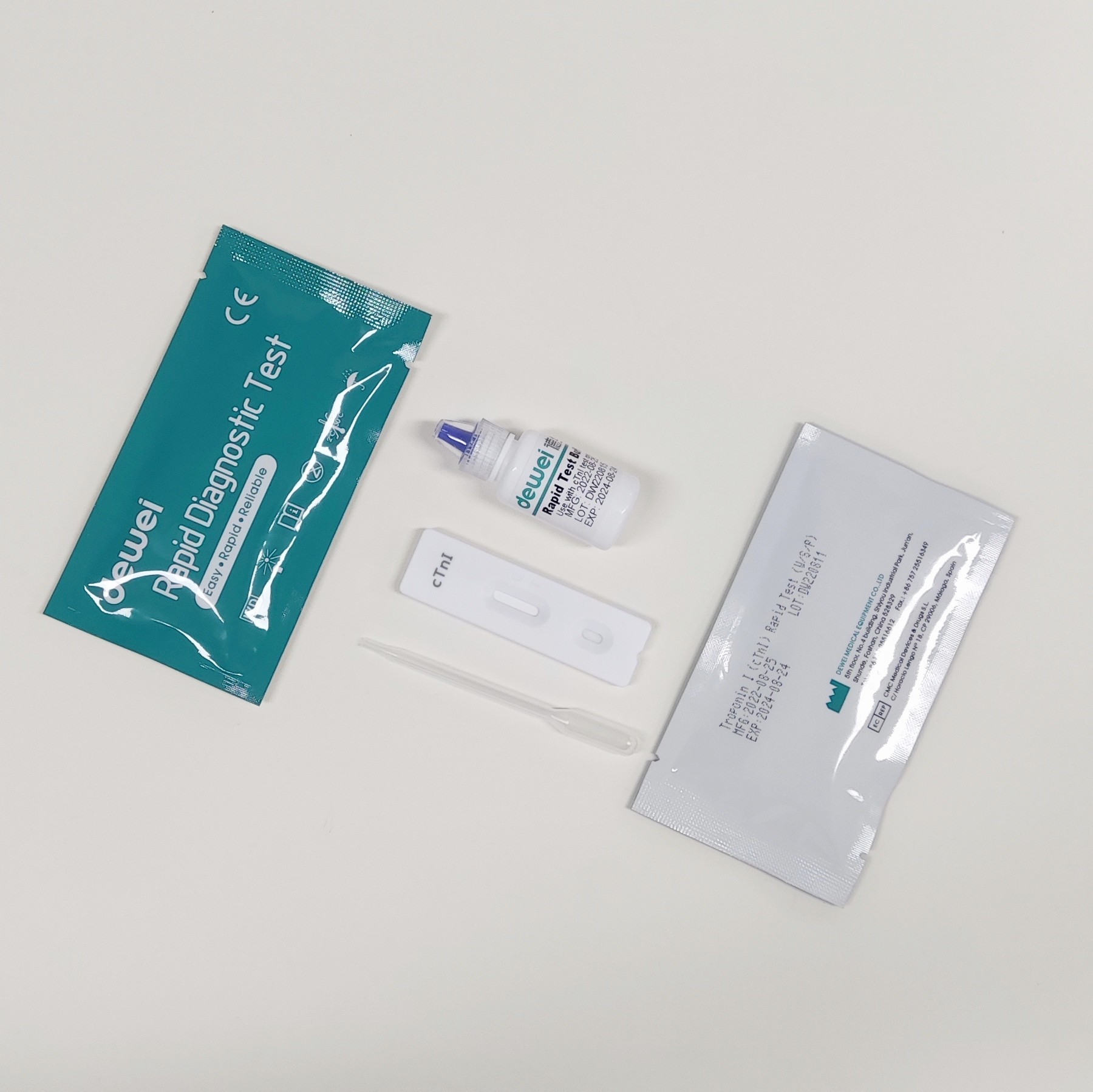
[Contenido principal]
• Cassette de prueba rápida con desecante
• Pipetas desechables
• Puerto de seguridad
• Folleto del producto
[Precauciones]
• Sólo para uso profesional de diagnóstico in vitro.
• No utilice después de la fecha de caducidad indicada en el envase.
• Este kit contiene productos de origen animal. El conocimiento certificado del origen y/o del estado sanitario de los animales no garantiza completamente la ausencia de agentes patógenos transmisibles.Por lo tanto,, se recomienda que estos productos se traten como potencialmente infecciosos y se manipulen siguiendo las precauciones de seguridad habituales (por ejemplo, no ingerir ni inhalar).
• Evitar la contaminación cruzada de las muestras utilizando un nuevo recipiente de recogida de muestras para cada muestra obtenida.
• Lea cuidadosamente todo el procedimiento antes de la prueba.
• No coma, beba ni fume en el área donde se manipulan las muestras y los kits.Observar las precauciones establecidas contra los peligros microbiológicos durante todo el procedimiento y seguir los procedimientos estándar para la eliminación adecuada de las muestras.. Usar ropa de protección como abrigos de laboratorio, guantes desechables y protección para los ojos cuando se analicen las muestras.
• La humedad y la temperatura pueden afectar negativamente a los resultados.
• Los materiales de ensayo utilizados deben desecharse de acuerdo con las normas locales.
[almacenamiento y estabilidad]
• Conservar a 2 ~ 30oC en la bolsa sellada durante 24 meses.
• Mantener alejado de la luz solar directa, la humedad y el calor
• NO congele.
[Colección de muestras]
•El Troponin I (cTnI) Rapid Test está destinado a ser utilizado únicamente con muestras de sangre humana, suero o plasma.
•Sólo se recomiendan muestras claras y no hemolisadas para este ensayo.
• Realice el ensayo inmediatamente después de la recogida de la muestra. No deje las muestras a temperatura ambiente durante períodos prolongados. Las muestras de suero y plasma pueden almacenarse a 2-8°C durante un máximo de 3 días.Para almacenamiento a largo plazoLa sangre entera recolectada por punción venosa debe almacenarse a 2-8°C si el análisis se va a realizar dentro de los 2 días siguientes a la recolección.Se debe analizar inmediatamente la sangre entera recolectada por puntillas..
•Se deben utilizar envases que contengan anticoagulantes como EDTA, citrato o heparina para almacenar sangre entera.
•Convierte las muestras a temperatura ambiente antes de realizar el ensayo. Las muestras congeladas deben descongelarse completamente y mezclarse bien antes del ensayo. Evite la congelación y descongelamiento repetidos de las muestras.
•Si los especímenes se van a enviar, empaquetarlos de conformidad con todas las normas aplicables para el transporte de agentes etiológicos. •Ictéricos, lipémicos, hemolisados,las muestras tratadas térmicamente y contaminadas pueden producir resultados erróneos.
•Existe una ligera posibilidad de que algunas muestras de sangre entera con una viscosidad muy alta o que se hayan almacenado durante más de 2 días no funcionen correctamente en el dispositivo de ensayo.Repita el ensayo con una muestra de suero o plasma del mismo paciente utilizando un nuevo dispositivo de ensayo.
[Dirección de uso]
Antes de su uso, los ensayos, las muestras, el amortiguador y/o los controles deben estar a temperatura ambiente (15-30°C).
1. Retire el ensayo de su bolsa sellada y colóquelo en una superficie limpia y plana.el ensayo debe realizarse dentro de una hora.
2Transfiera 1 gota de muestra de sangre entera, suero o plasma al pozo de muestra (S) del dispositivo con la pipeta desechable proporcionada, luego añada 1 gota de tampón y inicie el temporizador.Evitar la captura de burbujas de aire en el pozo de la muestra (S)A medida que la prueba comienza a funcionar, el color migrará a través de la membrana.
3. Espere a que aparezcan las bandas de color. El resultado debe leerse dentro de los 15 minutos. No interprete el resultado después de los 20 minutos.
[Interpretación de los resultados]
Positivo: la presencia de dos líneas como línea de control (C) y línea de ensayo (T) dentro de la ventana de resultados indica un resultado positivo.
NEGATIVO: la presencia de una sola línea de control (C) en la ventana de resultados indica un resultado negativo.Si la línea de control (C) no es visible dentro de la ventana de resultados después de realizar el ensayoAlgunas causas de resultados inválidos se deben a que no se siguen correctamente las instrucciones o al hecho de que la prueba se ha deteriorado más allá de la fecha de caducidad.Se recomienda volver a ensayar la muestra con un nuevo ensayo..
[CONTROL DE LA CALIDAD]
• Los controles internos de procedimiento se incluyen en el ensayo. Una banda de color que aparece en la región de control (C) se considera un control interno de procedimiento positivo.que confirme un volumen de muestra suficiente y una técnica procedimental correcta.
• Los controles externos no están incluidos en este kit.Se recomienda que los controles positivos y negativos sean probados como buena práctica de laboratorio para confirmar el procedimiento de ensayo y verificar el correcto desempeño del ensayo..
[Limitaciones]
1La prueba rápida cTnI es para uso profesional de diagnóstico in vitro y sólo debe utilizarse para la detección cualitativa de la troponina cardíaca I.No se deben deducir significados de la intensidad del color o del ancho de las bandas aparentes..
2La prueba rápida cTnI sólo indicará la presencia de troponina en la muestra y no debe utilizarse como único criterio para el diagnóstico de infarto de miocardio.
3Si el resultado de la prueba es negativo y persisten los síntomas clínicos, se recomienda realizar pruebas adicionales con otros métodos clínicos.un resultado negativo no excluye en ningún momento la presencia de troponina I en la sangre, porque los anticuerpos pueden estar ausentes o por debajo del nivel mínimo de detección del ensayo.
4Al igual que con todas las pruebas de diagnóstico, un diagnóstico confirmado sólo debe ser hecho por un médico después de que se hayan evaluado todos los resultados clínicos y de laboratorio.
5Algunas muestras que contienen títulos inusualmente elevados de anticuerpos heterófilos con factor reumatoide (RF) pueden afectar a los resultados esperados.La evaluación clínica adicional debe considerarse con otra información clínica disponible para el médico..
[Características de rendimiento]
Sensibilidad relativa: 99,45%
Especificidad relativa: 99,52%
Acuerdo general: 99,49%

 ¡Su mensaje debe tener entre 20 y 3.000 caracteres!
¡Su mensaje debe tener entre 20 y 3.000 caracteres! ¡Por favor revise su correo electrónico!
¡Por favor revise su correo electrónico!  ¡Su mensaje debe tener entre 20 y 3.000 caracteres!
¡Su mensaje debe tener entre 20 y 3.000 caracteres! ¡Por favor revise su correo electrónico!
¡Por favor revise su correo electrónico!